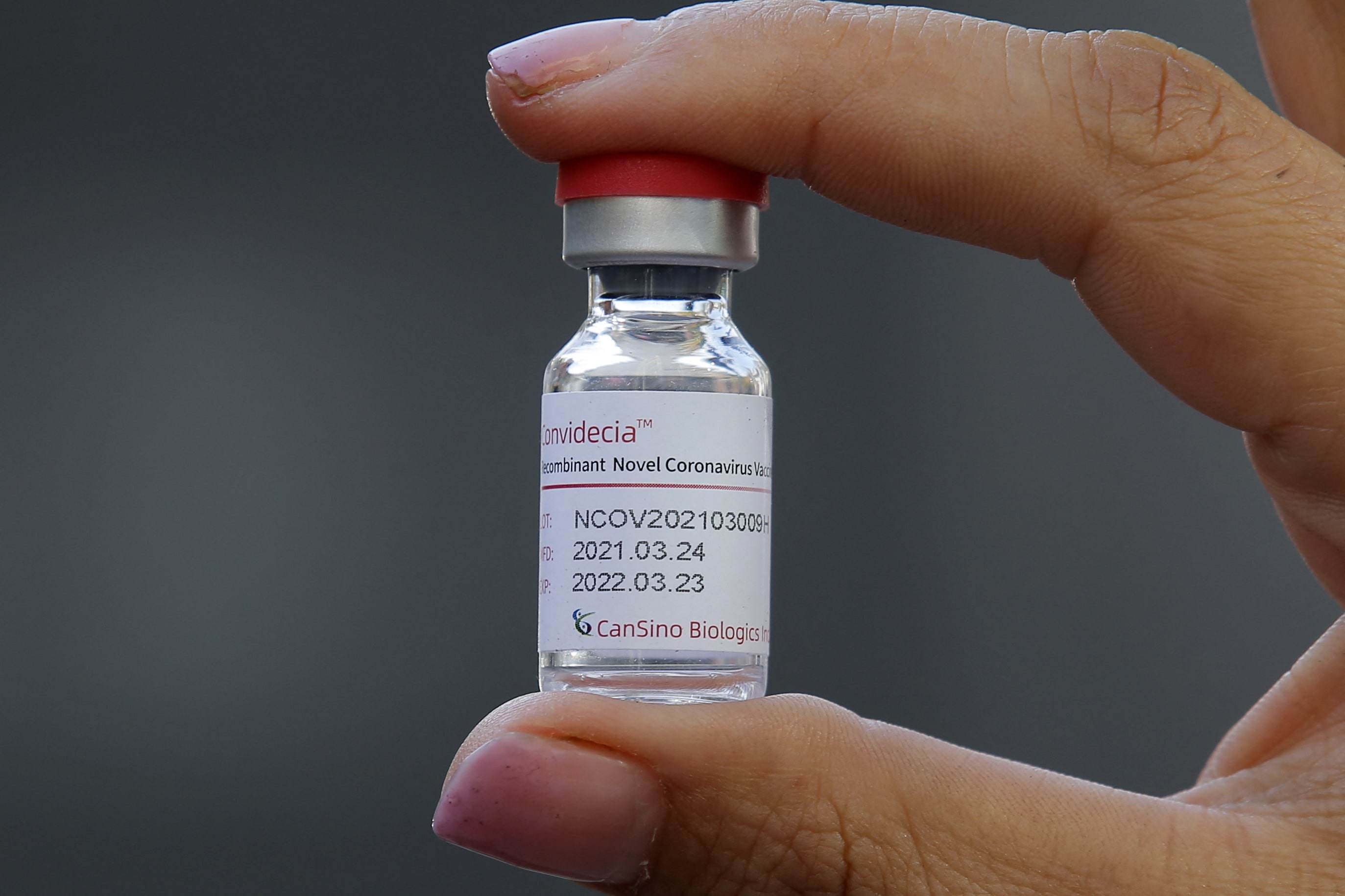
Anvisa encerra a análise do pedido de uso emergencial da vacina da CanSino
Em nota, a agência informou que o processo foi encerrado após a fabricante chinesa romper com sua representante no Brasil; mérito não foi avaliado
A Anvisa (Agência Nacional de Vigilância Sanitária) anunciou, na noite desta segunda-feira (28), em nota, que sua diretoria colegiada decidiu, por unanimidade, encerrar hoje o processo de análise da autorização temporária de uso emergencial, em caráter experimental, da vacina chinesa da CanSino, após um desacordo entre a fabricante chinesa e sua representante no Brasil.
Em nota, a agência informou que o processo foi encerrado “sem a continuidade da avaliação de mérito do pedido”, que foi feito pela então representante do imunizante no país, a Belcher Farmacêutica, no dia 18 de maio de 2021.
Falta de acordo
De acordo com a Anvisa, a Gerência Geral de Medicamentos e Produtos Biológicos da agência foi notificada por e-mail, no dia 17 de junho de 2021 — pouco menos de um mês depois de o pedido de autorização ser protocolado –, pela Cansino Biologics Inc., que a Belcher Farmacêutica e o Instituto Vital Brazil S.A. não possuíam mais autorização para representar a empresa no Brasil.
A Anvisa afirma que no dia seguinte, 18 de junho, informou ao Ministério da Saúde sobre o comunicado da Cansino Biologics e que, no dia 21, se reuniu com representantes da Belcher, que afirmaram que a situação era um “dissenso comercial” e solicitaram um prazo para se manifestar sobre o imbróglio.
O comunicado da Anvisa afirma que, no dia 22 de junho, a Belcher ratificou a revogação do contrato de representação da Cansino, e que, no dia 27, a farmacêutica chinesa confirmou que a companhia brasileira não mais a representava.
Fim do acordo encerrou o processo
Com o fim do acordo entre a Belcher e a Cansino, o processo foi finalizado por “ausência de condições para manutenção da continuidade da avaliação do pedido”, segundo a Anvisa.
“A perda de legitimidade processual da empresa Belcher Farmacêutica do Brasil Ltda e do Instituto Vital Brazil S.A. para atuar perante esta Agência por autorização da empresa Cansino Biologics Inc. enseja a ausência de condições para manutenção da continuidade da avaliação do pedido de autorização de uso emergencial da vacina CONVIDECIA perante a Anvisa. Aplica-se, ao caso, o disposto no inciso I do art. 9º da Lei nº 9.784/99, por perda de legitimidade da empresa Belcher Farmacêutica do Brasil Ltda e do Instituto Vital Brazil S.A. para atuarem interessados no presente processo administrativo”, disse a agência em nota.
A Anvisa afirma também que a Cansino solicitou a substituição do seu representante nacional, mas que a “ação não se figura como alternativa administrativamente viável”. Agora, um novo pedido de análise deverá ser protocolado para que a vacina seja analisada pela agência.
Ainda segundo a agência, a Belcher também pode solicitar nova análise da vacina, “desde que sanada a contestação de representação junto ao fabricante”.
Compra da vacina sob suspeita
A negociação da CanSino pode ser investigada pela CPI da Pandemia. O processo de aquisição do imunizante chinês foi similar ao da indiana Covaxin: com um intermediário e o preço por dose mais alto, de US$ 17– o maior dentre todas as vacinas adquiridas pelo Ministério da Saúde.
O Ministério da Saúde assinou a intenção de compra em 15 de junho, em um contrato de mais de R$ 5 bilhões por 60 milhões de doses. O acordo foi fechado com a então representante da farmacêutica chinesa no Brasil, a Belcher Farmacêutica.
A Belcher já foi alvo de investigação da operação Falso Negativo da Polícia Federal, que investiga a dispensa de licitação, superfaturamento e a baixa qualidade de testes para Covid-19 comprados pelo Distrito Federal.
Em nota, a empresa disse estar “à disposição para prestar esclarecimentos e colaborar com os trabalhos e investigações da CPI da Pandemia”, e que agiu sempre com boa-fé e ética.
A companhia afirmou ainda que não representa a CanSino desde o dia 10 deste mês “por questões técnicas de natureza privada entre as empresas”.
“A Belcher Farmacêutica informa, ainda, não ter firmado qualquer tipo de contrato com o Ministério da Saúde. E considerando que não mais representa no Brasil há cerca de 20 dias o laboratório chinês CanSino Biologics, não participará de eventuais novas fases de negociação ou contratualização”, diz o texto. “O documento referido, no entanto, não é vinculativo, não obriga a contratação por parte do poder público, tampouco o fornecimento pelo laboratório chinês.”