Anvisa cobra dados sobre Coronavac em crianças; Butantan diz que enviou dossiês
Está suspenso o prazo de 30 dias da agência reguladora para análise do pedido de autorização para vacinação contra Covid-19 da faixa etária de 3 a 17 anos


A Anvisa solicitou nesta quarta-feira (22) ao Instituto Butantan que sejam enviados mais dados sobre a utilização da vacina contra Covid-19, Coronavac, em crianças. O Butantan disse ter sido surpreendido, e que já enviou dossiês à agência.
“A solicitação é parte do processo de análise do pedido de autorização da Coronavac para a faixa de 3 a 17 anos”, informou a Anvisa em comunicado. O pedido foi feito pelo Butantan no último dia 15.
Embora a cobrança, desta quarta (22), não interrompa a análise dos técnicos sobre os dados já submetidos, a agência informou que está suspenso o prazo de 30 dias para avaliar o processo completo.
De acordo com a Anvisa, o novo pedido foi feito por orientação da área técnica da agência e especialistas externos das áreas médicas de imunologia e pediatria.
O grupo apontou a ausência de dados importantes para “afirmar de forma científica o grau de imunidade gerado nas crianças e adolescentes”.
A Anvisa destacou dois pontos que os dados irão responder:
- “Dados de ponte imunológica para a extrapolação da eficácia da vacina em adultos para crianças.”
- “Dados de segurança por faixa etária pediátrica, que envolve a entrega de dados separados por faixa etária.”
Butantan diz ter sido surpreendido
Em nota, o Instituto Butantan disse que foi, “mais uma vez”, surpreendido ao descobrir pela imprensa da decisão da Anvisa.
“Justamente na semana passada, enviamos separadamente dois dossiês com cinco novos estudos, além de dados de farmacovigilância e de segurança vindos da Sinovac, biofarmecêutica chinesa produtora da CoronaVac, e do governo chileno”, argumenta o Butantan.
O comunicado ainda afirma que um terceiro dossiês, com os dados da fase 3 de estudo do imunizante, foi enviado separadamente.
O Instituto destaca que foi feita uma reunião entre especialistas do Butantan, das principais sociedades médicas pediátricas do país e membros da Anvisa.
O encontro teria sido “para tirar as dúvidas dos estudos e ratificar a estratégia de que a Coronavac é a vacina mais recomendada para a faixa etária de 3 a 17 anos”.
O Butantan alega que, na reunião, a agência reguladora não fez questionamentos.
“É preciso que haja mais clareza por parte da Anvisa para que assuntos como a aprovação da vacina no contexto pandêmico que vivemos sejam tratados com a rapidez necessária”, conclui o comunicado.
Em nota, a Anvisa diz que emitiu uma exigência para o Instituto Butantan no dia 22 de dezembro. “O Butantan, em resposta, enviou documentos que estão em análise pela Anvisa. Não temos como antecipar previsões ou conclusões antes do encerramento do processo. A decisão da Anvisa sobre qualquer vacina ou medicamento é feito na conclusão do processo”, informa a agência.
-
 1 de 16
1 de 16Posto de vacinação no Museu da República, no Catete, no Rio de Janeiro. Veja a vacinação contra a Covid-19 no Brasil e no mundo • Pedro Duran/CNN
-
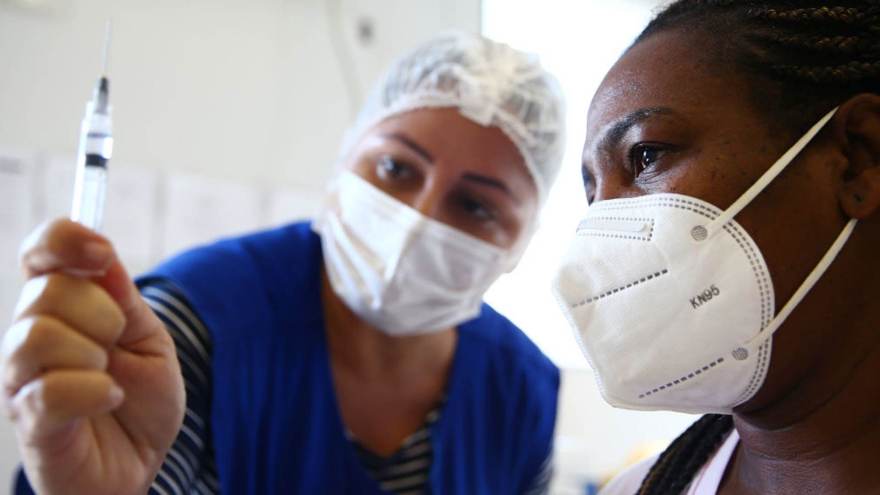 2 de 16
2 de 16Enfermeira mostra vacina contra a Covid-19 para mulher no Rio de Janeiro • Mario Tama/Getty Images
-
 3 de 16
3 de 16Enfermeira do SUS aplica vacina contra Covid-19 em homem em sua casa na Rocinha, no Rio, em uma das rondas frequentes que profissionais de saúde fazem na comunidade para imunizar pessoas que não querem ir ao posto • Mario Tama/Getty Images
-
-
 4 de 16
4 de 16Vacinação contra a Covid-19 em São Paulo • Reuters/Carla Carniel
-
 5 de 16
5 de 16Enfermeira na campanha de vacinação contra a Covid-19 na Ilha de Paquetá, no Rio de Janeiro • Fernando Souza/picture alliance via Getty Images
-
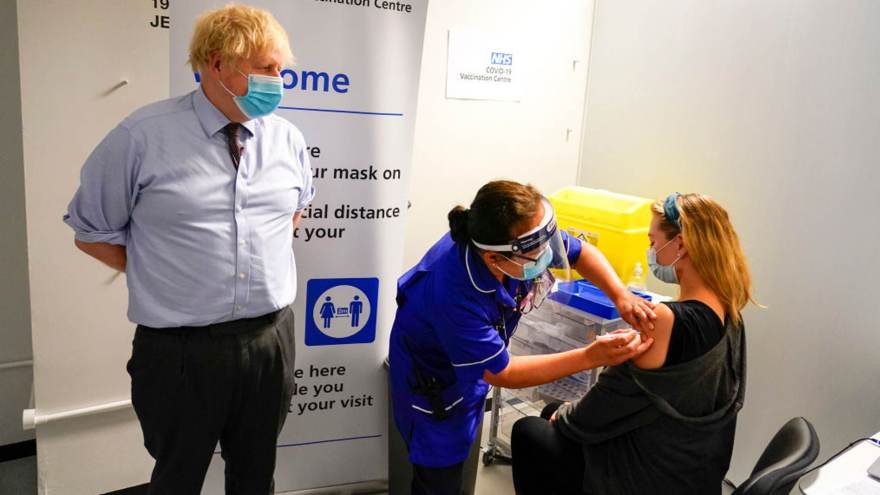 6 de 16
6 de 16Boris Johnson visita centro de vacinação contra a Covid-19 em Londres • Alberto Pezzali - WPA Pool/Getty Images
-
-
 7 de 16
7 de 16Japonesa faz triagem para ser vacinada contra Covid-19 • Stanislav Kogiku - 2.ago.2021/Pool Photo via AP
-
 8 de 16
8 de 16China vacina estudantes universitários contra a Covid-19 • Costfoto/Barcroft Media via Getty Images
-
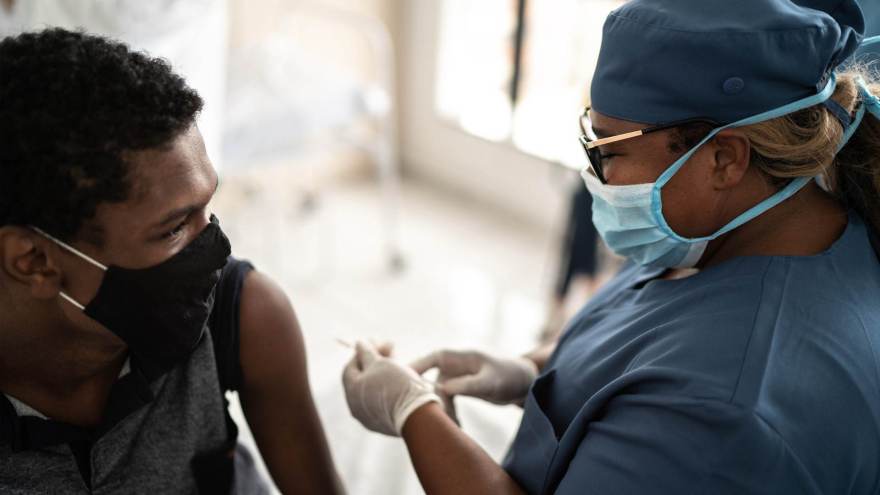 9 de 16
9 de 16Alguns países já fazem a vacinação de adolescentes contra a Covid-19 • Getty Images (FG Trade)
-
-
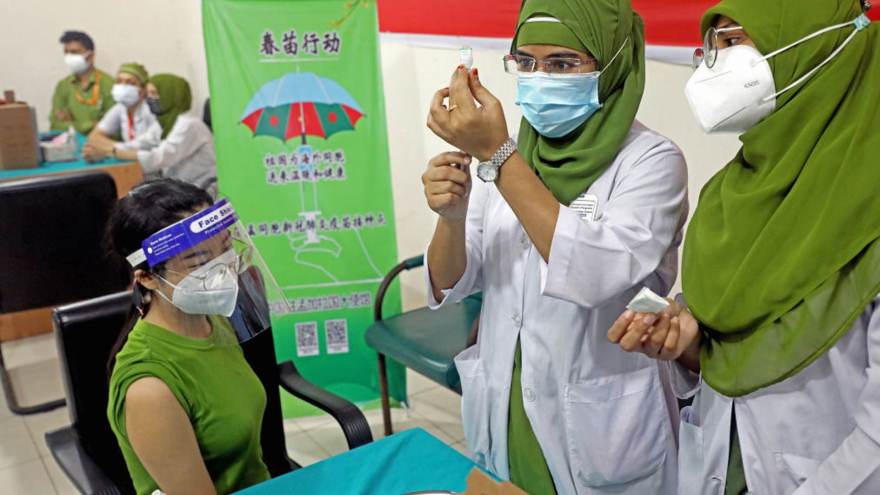 10 de 16
10 de 16Enfermeira aplica vacina em Dhaka, Bangladesh, que pretende imunizar 10 milhões em uma semana • Maruf Rahman / Eyepix Group/Barcroft Media via Getty Images
-
 11 de 16
11 de 16Cidade de Aue-Bad Schlema, na Alemanha, distribui cachorros-quentes gratuitamente para quem apresentar o cartão de vacinação • Hendrik Schmidt/picture alliance via Getty Images
-
 12 de 16
12 de 16Vacinação contra Covid-19 em Nova Délhi, na Índia • Adnan Abidi/Reuters
-
-
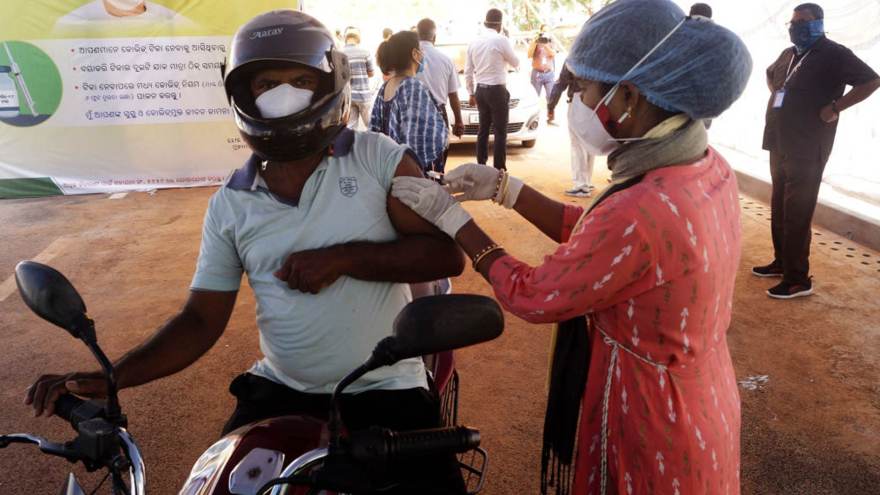 13 de 16
13 de 16Homem de 45 anos é vacinado em posto drive-in na cidade de Bhubaneswar, na Índia • STR/NurPhoto via Getty Images
-
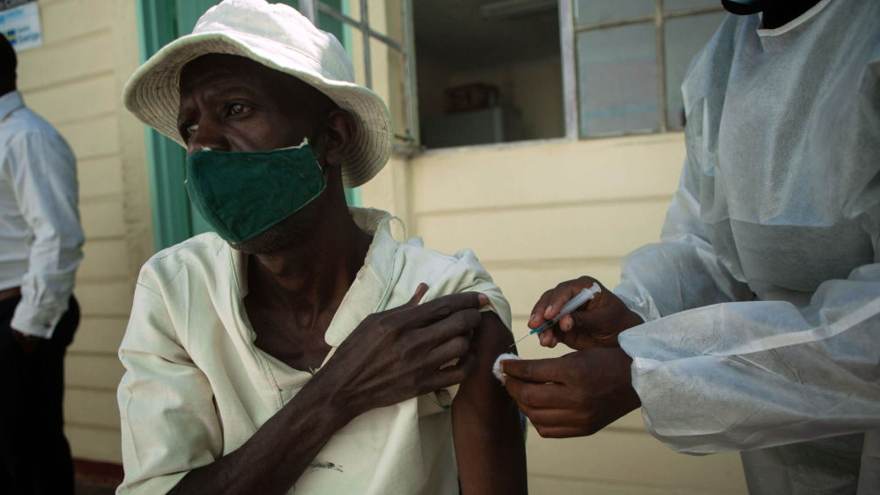 14 de 16
14 de 16Vacinação contra a Covid-19 em prisão em Harare, Zimbabwe • Tafadzwa Ufumeli/Getty Images
-
 15 de 16
15 de 16Vacinação contra a Covid-19 em Dakar, no Senegal • Fatma Esma Arslan/Anadolu Agency via Getty Images
-
-
 16 de 16
16 de 16Vacinação contra a Covid-19 em Bangcoc, Tailândia • Reuters/Athit Perawongmetha










