Anvisa autoriza testes de quarta vacina contra Covid-19 no país
Estudo clínico da vacina da Johnson & Johnson começou em julho nos Estados Unidos e na Bélgica, e agora se encontra na terceira fase


A Agência Nacional de Vigilância Sanitária (Anvisa) publicou, no Diário Oficial de hoje (18), autorização da realização de testes com a vacina desenvolvida pela empresa Janssen, farmacêutica da Johnson & Johnson, para Covid-19.
Conforme antecipou a CNN, Os primeiros testes devem começar pelo estado de São Paulo. A ideia é que as pessoas testadas sejam voluntários com maior risco de exposição ao novo coronavírus.
Leia mais:
Quem pode ser voluntário nos testes de vacinas contra a Covid-19 no Brasil
Quem vai receber a vacina contra a Covid-19 primeiro quando ela for aprovada?
Por que tantos testes de vacina estão acontecendo no Brasil?
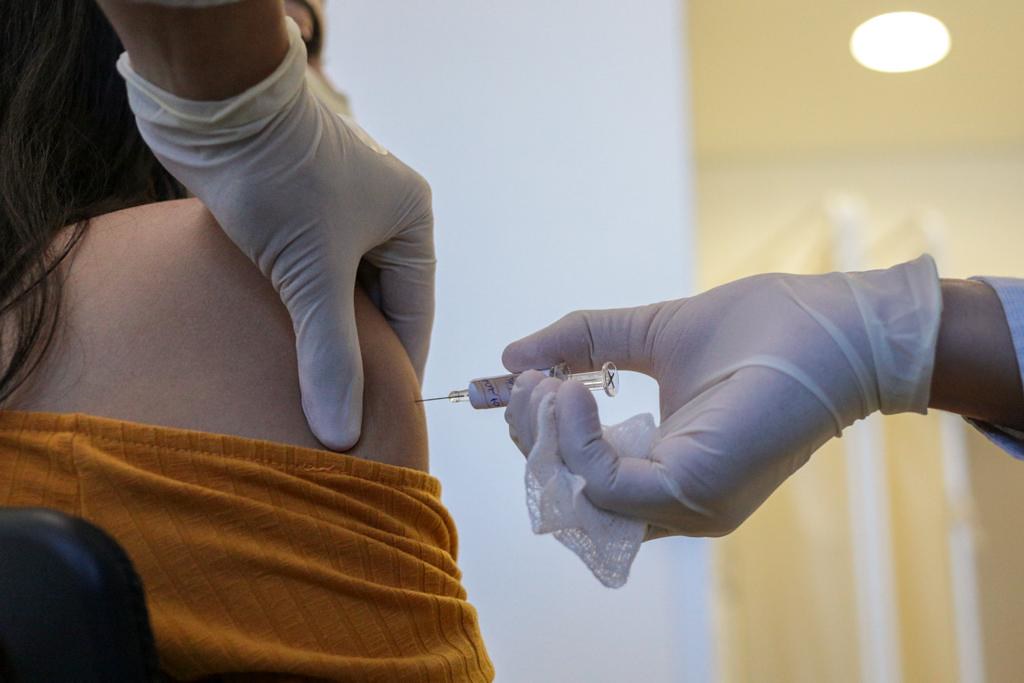
O Brasil será um dos países participantes desta etapa, com previsão de participação de até 60 mil voluntários.
Em nota, a Janssen diz que a fase 3 será conduzida globalmente com até 60 mil voluntários saudáveis, com idades entre 18 e 60 anos, e deve começar em setembro.
No Brasil, 7 mil voluntários devem ser testados em 20 centros, localizados nos estados de São Paulo, Rio de Janeiro, Rio Grande do Norte, Minas Gerais, Rio Grande do Sul, Bahia e Paraná.
Este é o quarto estudo de vacina contra o novo coronavírus autorizado pela Anvisa no Brasil. Anteriormente, a Agência autorizou o ensaio clínico das vacinas desenvolvidas pela Universidade de Oxford, no Reino Unido, pela empresa Sinovac Research & Development Co. Ltd. em parceria com o Instituto Butantan e pela BioNTech e Wyeth/Pfizer.
Ministério da Saúde
Em nota, o Ministério da Saúde afirmou que “está atento aos estudos e a todas as vacinas em desenvolvimento e garante que, assim que tiver acesso à vacina comprovadamente eficaz contra a Covid-19, colocará à disposição dos brasileiros”.










